Microbioma intestinal y Alzheimer
La microbiota intestinal desempeña un papel esencial en el desarrollo y la maduración del sistema inmunológico (Angelucci et al. 2019). Diversos estudios han demostrado que una mayor diversidad microbiana está asociada con una mejor salud general (Romanenko et al. 2021). Entre sus funciones clave, la microbiota intestinal produce moléculas neuroprotectoras como ácidos grasos de cadena corta (butirato y acetato) y antioxidantes (Angelucci et al. 2019). Sin embargo, un desequilibrio en esta comunidad microbiana, conocido como disbiosis, se ha relacionado recientemente con procesos neurodegenerativos (Romanenko et al. 2021).
La disbiosis intestinal puede inducir neuroinflamación, reducir la expresión del factor neurotrófico derivado del cerebro (BDNF) y del receptor NMDA, lo cual favorece el deterioro cognitivo, trastornos del estado de ánimo y niveles elevados de beta-amiloide (Aβ), debido al aumento de la permeabilidad intestinal (Imagen 1) (Angelucci et al. 2019; Romanenko et al. 2021)
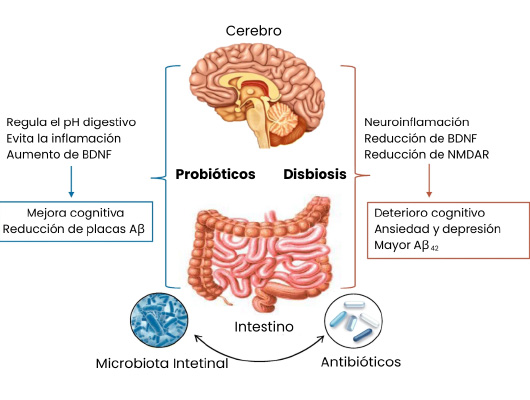
Imagen 1. Representación esquemática del papel del eje microbiota-intestino-cerebro en la enfermedad de Alzheimer (modificado de Angelucci, 2019).
La enfermedad de Alzheimer, la forma más común de demencia en la vejez, se caracteriza por un deterioro progresivo de las funciones cognitivas, pérdida de neuronas y sinapsis específicas. Esta patología es multifactorial, influenciada por factores genéticos, vasculares, de estilo de vida y ambientales (Grabrucker et al. 2023). En los últimos años, se ha identificado una estrecha relación entre el Alzheimer y la microbiota intestinal, lo que ha dado origen al concepto del eje microbiota-intestino-cerebro, un sistema de comunicación bidireccional que integra señales neuronales, inmunológicas, endocrinas y metabólicas (Romanenko et al. 2021).
Aunque inicialmente fue considerada una hipótesis, hoy en día el eje microbiota-intestino-cerebro está respaldado por abundante evidencia clínica y preclínica. Cambios en la composición de la microbiota intestinal se han asociado no solo con ansiedad y depresión, sino también con enfermedades neurodegenerativas como el Alzheimer y la epilepsia farmacorresistente (Angelucci et al. 2019; Romanenko et al. 2021).
En pacientes con Alzheimer, se ha observado un aumento en bacterias de los filos Proteobacteria y Bacteroidetes, junto con una disminución de Firmicutes y Actinobacteria, en comparación con personas cognitivamente sanas (Romanenko et al. 2021). Asimismo, se han detectado alteraciones en grupos específicos como Bacteroides, Ruminococcus, Lachnospiraceae, Actinobacteria y Selenomonadales (Romanenko et al. 2021). También se ha identificado una menor presencia de bacterias productoras de butirato, un metabolito clave que está negativamente asociado con la acumulación de amiloide cortical (Grabrucker et al. 2023).
Cualquier factor que altera la microbiota intestinal puede actuar como desencadenante de trastornos neurológicos, incluido la enfermedad de Alzheimer (Angelucci et al. 2019; Romanenko et al. 2021). Estudios recientes en humanos han mostrado que infecciones virales o bacterianas —como Helicobacter pylori, Porphyromonas gingivalis, Candida albicans, Candida glabrata, virus del herpes simple, VIH o citomegalovirus— pueden influir en la fisiopatología del Alzheimer mediante la liberación de citocinas proinflamatorias y la inducción de estrés oxidativo (Romanenko et al. 2021).
Además, hasta un 81 % de los pacientes con Alzheimer también presentan diabetes tipo 2 (DM2), y se ha demostrado que la resistencia a la insulina y la hiperinsulinemia inducen inflamación y elevan la expresión de mediadores proinflamatorios, lo cual favorece el desarrollo de Alzheimer (Romanenko et al. 2021).
El uso prolongado de antibióticos de amplio espectro también se ha vinculado con trastornos neurológicos como ansiedad, depresión, psicosis o delirio, al alterar negativamente la diversidad microbiana intestinal y favorecer el deterioro neurológico (Angelucci et al. 2019; Romanenko et al. 2021). Incluso estudios preclínicos con antibióticos han demostrado que la microbiota regula la producción de mielina en la corteza prefrontal en modelos animales (Imagen 1) (Angelucci et al. 2019).
Por otro lado, la suplementación dietética con probióticos ha mostrado beneficios no solo para mantener la actividad cerebral normal, sino también para revertir alteraciones cognitivas en pacientes con Alzheimer (Angelucci et al. 2019). Estos efectos positivos se deben a la capacidad de los probióticos para estabilizar el pH intestinal, reducir la inflamación y potenciar la producción de moléculas neuroprotectoras (Imagen 2) (Romanenko et al. 2021).
Por eso, realizar un test de microbiota intestinal es clave para detectar posibles desequilibrios que podrían estar afectando tu salud cerebral y cognitiva. Con nuestro servicio, obtendrás un análisis completo de tu microbiota y recomendaciones personalizadas en alimentación, uso de probióticos y estilo de vida. Anticípate, cuida tu salud intestinal y previene desde ahora trastornos neurológicos. Tu bienestar empieza en el intestino, y nosotros te ayudamos a entenderlo.
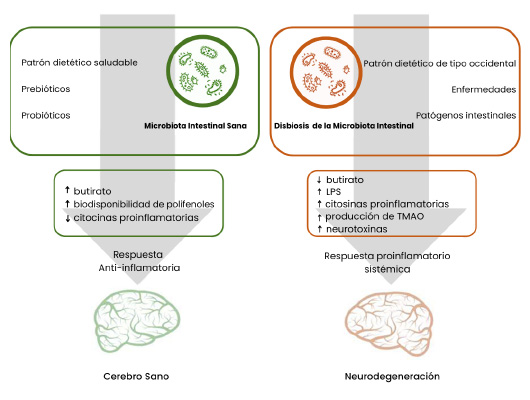
Imagen 2. El papel de la nutrición y la microbiota intestinal en la patogénesis de la enfermedad de Alzheimer (modificado de Romanenko, 2021).
Referencias
Angelucci, F., Cechova, K., Amlerova, J., & Hort, J. (2019). Antibiotics, gut microbiota, and Alzheimer’s disease. Journal of neuroinflammation, 16, 1-10.
Grabrucker, S., Marizzoni, M., Silajdžić, E., Lopizzo, N., Mombelli, E., Nicolas, S., et al. (2023). Microbiota from Alzheimer’s patients induce deficits in cognition and hippocampal neurogenesis. Brain, 146(12), 4916-4934.
Romanenko, M., Kholin, V., Koliada, A., & Vaiserman, A. (2021). Nutrition, gut microbiota, and Alzheimer’s disease. Frontiers in psychiatry, 12, 712673.
Jiang, C., Li, G., Huang, P., Liu, Z., & Zhao, B. (2017). The gut microbiota and Alzheimer’s disease. Journal of Alzheimer’s Disease, 58(1), 1-15.